RNA干扰(RNA interference,RNAi)是双链RNA(Double-stranded RNA,dsRNA)启动的序列特异性基因沉默的保守过程,被广泛用作基因功能研究,潜在RNA治疗和农业害虫防治的重要工具。RNAi最初在秀丽隐杆线虫(Caenorhabditis elegans,C. elegans)中发现的,随后研究表明也广泛存在于植物、真菌和后生动物中。有趣的是,C. elegans存在系统性RNA干扰(Systemic RNAi),即基因沉默信号可以在细胞和组织间进行传递。实验证据表明在系统性RNA干扰缺陷(Systemic RNA interference defects,SID)位点中,跨膜蛋白SID-1对于dsRNA在细胞间的摄取和传播是必不可少的。SID-1在大多数动物中都有保守的同源物,其中人源同源蛋白SIDT1和SIDT2参与包括自噬、免疫反应和代谢等多种生理过程,其失调或者突变可导致多种人类疾病。但SID-1家族蛋白结合和转运dsRNA的机制尚不清楚:(1)SID-1如何特异性识别dsRNA而非DNA;(2)“SID-1蛋白是dsRNA通道”假说缺乏直接的结构证据;(3)SID-1蛋白介导dsRNA摄取和转运的分子机制也不清晰。
中国科学院物理研究所/北京凝聚态物理国家研究中心软物质物理实验室SM10组姜道华研究团队,结合生物物理和生物化学等方法长期致力于疾病相关的离子通道蛋白[Cell, 184, 5151 (2021); Cell Reports, 37 (2021); Nat Commun. 13, 1286 (2022); Nat Commun. 13, 2713 (2022); Nat Struct & Mol Biol, 29, 1208 (2022); Nat Chem Biol, 19, 81 (2023); Nat Commun. 14, 1030 (2023); Cell Reports, 42 (2023)]和转运蛋白[Nature, 626, 427 (2024)]结构与功能的研究,并取得了系列成果。
2024年4月25日,姜道华研究团队和华中科技大学龚健科教授团队在国际期刊Nature Structural & Molecular Biology发表题为“Structural insights into double-stranded RNA recognition and transport by SID-1”的学术论文。通过单颗粒冷冻电镜技术解析了线虫SID-1以及人源SIDT1和SIDT2蛋白高分辨率结构(图1a),发现SID-1以保守的同源二聚体形式存在,其二聚体形式和保守的Zn2+位点在SID-1介导的dsRNA摄取中起关键作用。研究人员进一步解析了SID-1/dsRNA复合物结构(图1b),dsRNA结合在胞外区ECDI和ECDII结构域之间,大约25bp长度的dsRNA与ECD直接相互作用。dsRNA与SID-1的结合并没有改变二聚体整体结构,不具有任何明显的溶剂可达通道,更没有可供dsRNA通过的孔径。因此,SID-1不是前人推测的dsRNA通道。此外,SID-1的 ECD三个正电区域I-III通过与dsRNA的磷酸基团的静电相互作用和dsRNA核糖2'-OH基团形成的氢键将dsRNA牢牢“抓住”,解释了SID-1蛋白特异性识别dsRNA而非dsDNA的匹配机制。
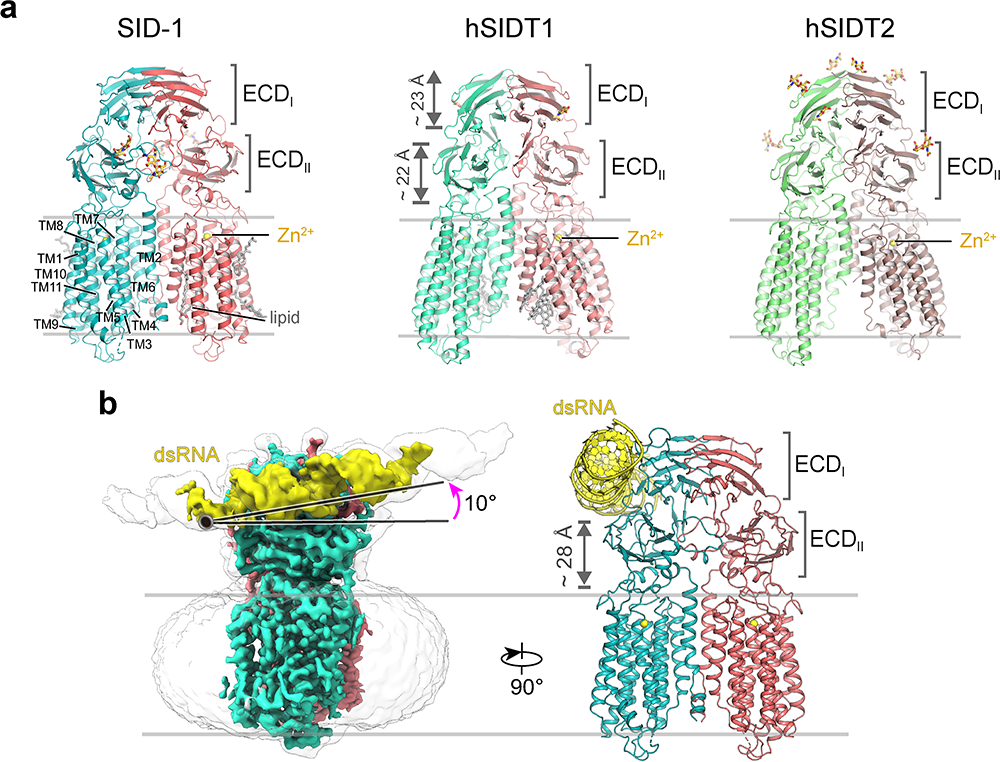
图1. SID-1的整体结构。a. SID-1,SIDT1和SIDT2蛋白结构模型;b. SID-1/dsRNA复合物电镜密度图和结构模型。
研究人员还探究了SID-1 的dsRNA转运机制(图2)。SID-1的Loop TM1-2在dsRNA摄取和转运中起着关键作用。Confocal共定位发现SID-1和dsRNA共定位于类似囊泡颗粒的亚细胞器中,推测SID-1作为dsRNA的受体,识别并结合细胞外dsRNA后,可能会进一步形成囊泡等亚细胞器,以内吞作用方式带着dsRNA进入细胞。结合dsRNA/SID-1复合物结构以及dsRNA转运机制的探究,最终提出了SID-1介导的系统性RNA干扰可能的工作模型。由于SID-1膜定位、对dsRNA的高特异性结合和囊泡内吞等特点,SID-1可能成为RNAi药物的载体,在RNA药物靶向递送技术如人工纳米载体、外泌体等方面有潜在的应用价值。
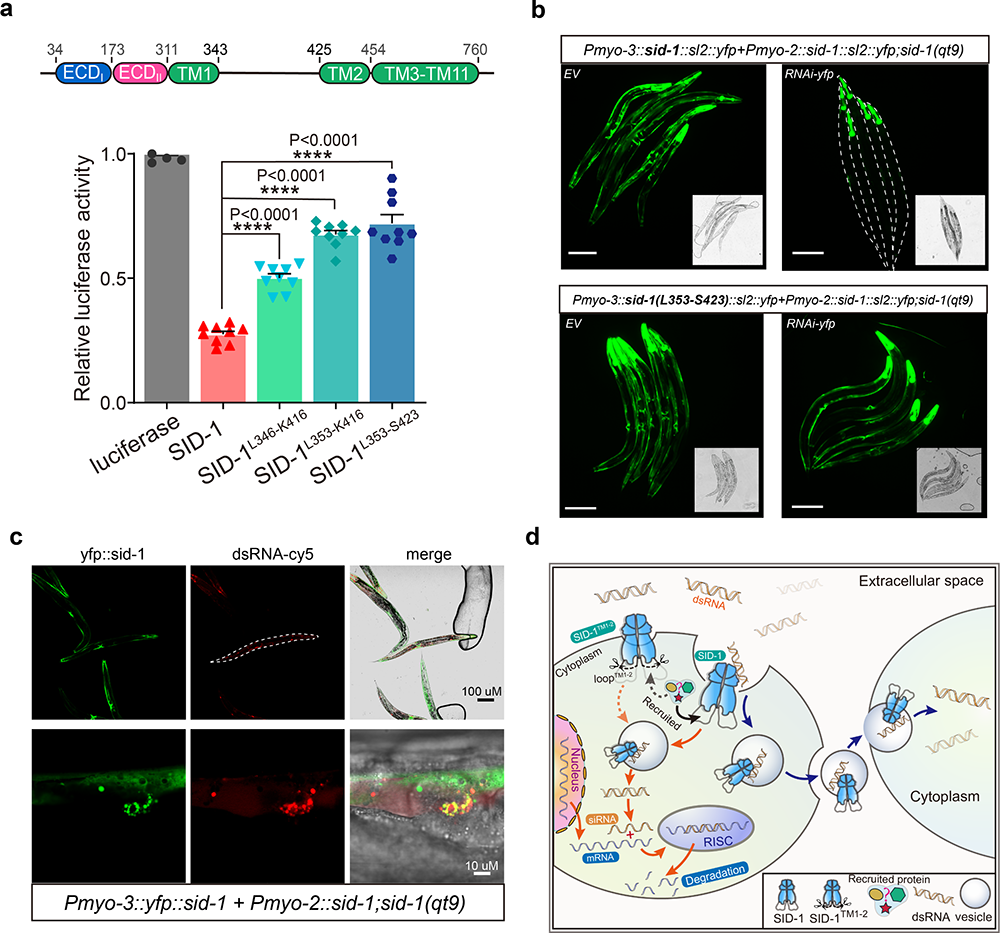
图2. SID-1的dsRNA转运机制
a. SID-1 TM1-2截短体的S2细胞dsRNA摄取实验; b. SID-1截短体系统性RNAi产生缺陷;c. Confocal共聚焦观察SID-1蛋白与dsRNA的共定位;d. SID-1介导的系统性RNA干扰可能的内吞工作模型。
中国科学院物理研究所姜道华特聘研究员和华中科技大学龚健科教授为本研究论文的共同通讯作者。华中科技大学与中国科学院物理研究所联合培养博士研究生张江涛,华中科技大学博士研究生展春华和硕士研究生伍点,北京大学特聘副研究员范俊萍和中国农业科学院博士研究生张瑞雪为共同第一作者。中国科学院物理研究所李明研究员,陆颖研究员,博士研究生武迪和陈昕瑶为本研究重要提供帮助。本研究获得了中国科学院和国家自然科学基金委员会的资助。
文章DOI号(https://doi.org/10.1038/s41594-024-01276-9)

